跨学科对话
如何识别血管炎导致的冠脉病变?(心血管医师必读)
主讲专家:吴炜;张闻多;于雪;李菁;陈玉国
讨论嘉宾:
报告会场:CMIT2018/MDT联合诊室/系统性血管炎
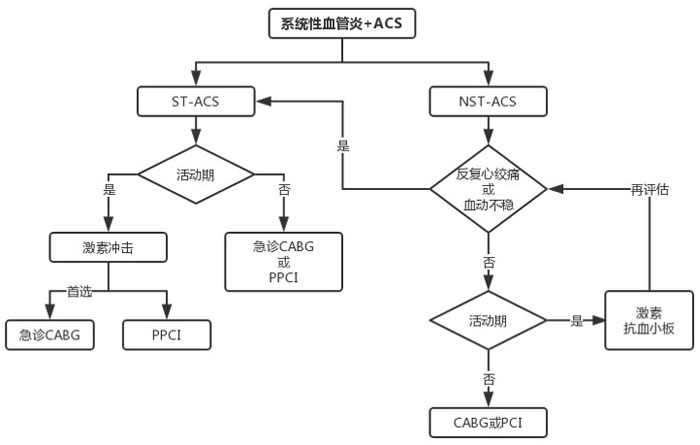
编者按系统性血管炎可合并冠脉病变,可以表现急重症,很多患者发病前没有基础疾病的治疗,提示我们应重视血管炎的诊治。心血管医师如何从冠脉严重病变中识别血管炎累及冠脉?不同血管炎的心血管表现有何不同?本期《CMIT周刊》邀请心血管、风湿免疫专家为大家讲解上述问题,敬请关注!
导入病例1
22岁男性,反复意识丧失3年余,活动后胸闷2年余,加重5月。
现病史
2012年4月行走时突发意识丧失,伴双眼凝视、口吐白沫、肢体抽搐,无舌咬伤、尿便失禁,约1小时意识自行恢复。上述症状于2012年底、2013年中再发2次,外院查脑电图、头颅MRI未见异常。
2013年6月起出现上2~3层楼后胸闷,休息数分钟可缓解,活动耐量进行性减低。
2014年10月卧位休息时再发意识丧失,性质同前,意识恢复后出现言语不利,右侧肢体麻木、肌力下降。外院查:
•BP160-170/110mmHg。心电图:窦性心律,HR 102bpm,II、III、aVF可见小Q波、ST段压低0.05mV、T波倒置。
•尿常规:Pro>3g/L,BLD(-),24小时尿蛋白4.9g;肝肾功(-);免疫球蛋白及补体:IgM↓0.293g/L,C4 0.405↑,余正常;自身抗体均(-)。
•头MRI:左侧中脑大脑脚长T1长T2,DWI高信号,考虑为新发梗死,左侧额叶半卵圆中心白质高信号。肌电图大致正常。
外院考虑“慢性肾小球肾炎,高血压,脑血管病”,予硝苯地平控释片、福辛普利钠降压,他克莫司早2mg/晚1mg治疗肾病,血压波动于140/90mmHg,针灸治疗后肢体活动不利及言语不清逐渐恢复。此后患者活动后胸闷、憋气症状仍进行性加重,2015年初出现步行数十米或上1层楼后胸痛,伴向双上肢放射,休息数分钟后可缓解。
2015年6月1日夜间患者突发胸痛,伴胸闷、憋气,不能平卧,双下肢对称可凹性水肿。cTnI 1.31ng/mL(6月3日)→7.7ng/ml(6月5日),NT-proBNP 778pg/ml。肺部CT:双肺少量斑片影。超声心动图:左室轻度增大,收缩功能减低(LVEF 36%)。予利尿治疗后症状略改善。
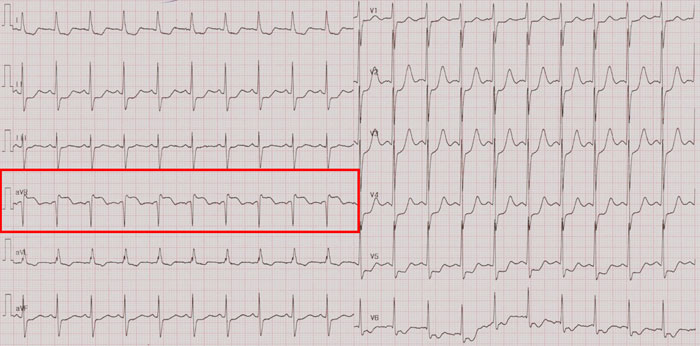
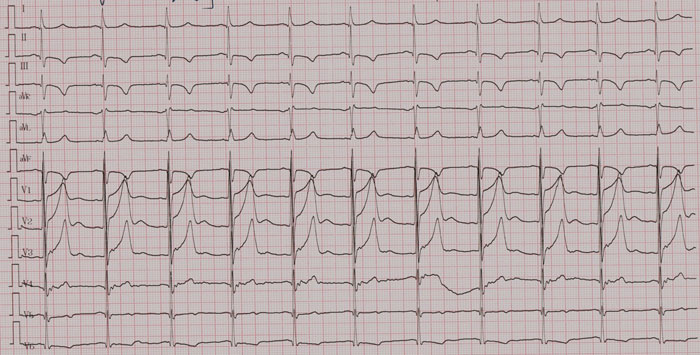
6月14日患者床旁活动后出现心前区痛、向双上肢放射伴胸闷、憋气,急诊就诊。查心电图示窦性心动过速,aVR ST段抬高0.2mV,I、aVL、II、aVF、V1-V7 ST段压低,I、aVL、V5-V7 T波双向或倒置,cTnI 1.74~4.67ug/L,考虑急性非ST段抬高心肌梗死,予阿司匹林、氯吡格雷、阿托伐他汀、低分子肝素治疗及硝酸甘油静脉泵入,症状持续2-3小时后缓解,收入CCU。(图1 胸痛发作时心电图)(图2 胸痛缓解时心电图)
既往史
儿时体健,无长期发热病史,2012年初出现发热,Tmax 39℃,伴有右侧腮腺区肿大,半月后出现后背部斑丘疹,伴破溃,20天左右好转;同年夏天出现左侧睾丸疼痛,间断发作,口服迈之灵可缓解。
个人史、家族史
无特殊,病前为校篮球队员。
【体格检查】
BP 120/60mmHg,HR 73bpm,BMI 25.9kg/m2,背部皮肤可见陈旧皮疹遗留色素沉着,腹部紫纹。心肺听诊(-),腹部(-),双侧上肢血压对称,足背动脉搏动双侧未及;右侧Hoffman(+),Babinski(+),左侧上下肢病理征未引出。
【实验室检查】
血常规(-)。
尿常规:PRO TRACE,BLD(-);24小时尿蛋白0.61-1.06g,98%肾小球来源。
肾功能:Cr 80-100μmol/L。
血脂:LDL-C 1.11mmol/L,TC 2.49mmol/L,TG 2.14mmol/L,HDL-C 0.70mmol/L。
心肌酶:cTnI最高6.1μg/L后逐渐下降;BNP 240ng/L。
炎症指标:hsCRP 5.92mg/L;ESR 49mm/h。
免疫指标:C3、C4、IgA、IgG、RF(-),IgM↓0.27g/L;ANA3项、抗ENA抗体、ANCA、LA、抗磷脂抗体谱均(-);乙肝5项:HBeAb、HBcAb、HBsAb(+),HBV-DNA(-)。
【辅助检查】
超声心动图:节段性室壁运动异常(左室下后壁内膜回声增强,无运动,室间隔基部运动减低),左室收缩功能减低,双平面法LVEF 42%,轻度二、三尖瓣关闭不全。
下肢动脉超声:右侧胫前动脉弥漫性狭窄,左侧胫前动脉中下段闭塞可能性大;双上肢超声未见明显狭窄。
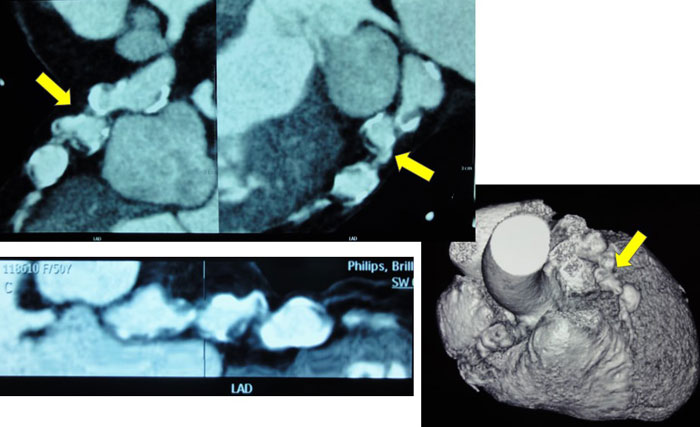
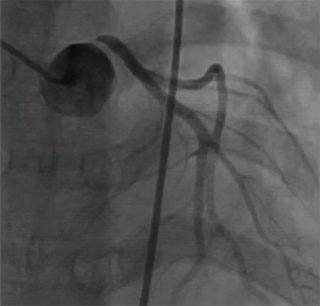
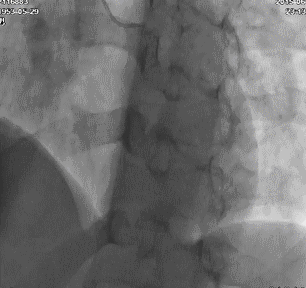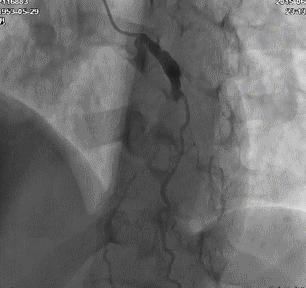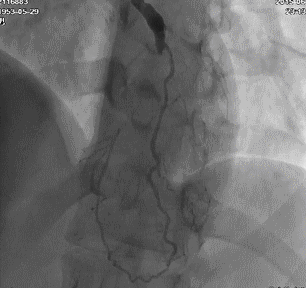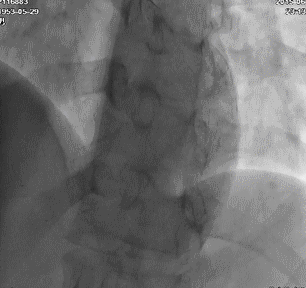
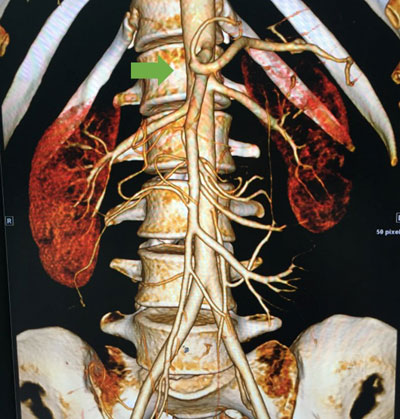
腹主动脉CTA:脾动脉及双肾动脉远端管腔轻度狭窄,可见小侧支循环开放。肝总动脉及其分支闭塞,周围多发细小侧支循环开放。肠系膜下动脉起始部及双侧髂内动脉多发管腔不同程度狭窄。考虑血管炎性病变可能;脾脏前下部片状低强化区,脾梗死可能;左肾小片状强化减低影,缺血性改变可能。(图3 腹主动脉CTA)
头颈CTA:右侧椎动脉全程闭塞;余头颈部血管未见明显异常。
神经内科会诊:反复意识丧失考虑癫痫发作,左侧中脑梗死可能为小血管闭塞所致,与高血压或全身血管炎相关。
免疫科会诊:考虑系统性血管炎,结节性多动脉炎可能性大。建议予泼尼松1mg/kg,环磷酰胺0.4g/周,并建议积极冠脉重建。
多科会诊(心外、心内、麻醉科):考虑患者冠脉病变有CABG指征,但病因为血管炎且尚未控制,外科手术风险极高,受益有限。介入治疗方面患者冠脉病变极重,仅一根对角支供应全部冠脉血供,一旦处理前降支导致对角支开口闭塞,治疗风险极大。
入院后逐步减停硝酸甘油泵入,给予阿司匹林100mg qd、氯吡格雷75mg Qd(1个月后停用),低分子肝素→华法林抗凝,单硝酸异山梨酯缓释片60mg qd、尼可地尔5mg tid、盐酸曲美他嗪20mg tid扩冠和改善心肌代谢,酒石酸美托洛尔95mg q12h降低心肌耗氧,福辛普利5mg qd、辛伐他汀20mg qn、呋塞米10mg qd、螺内酯20mg qd。
甲强龙60mg iv qd×7d→泼尼松60mg qd;环磷酰胺0.4g qw。
整体评价后未进行再血管化治疗。
患者病情相对平稳后出院,泼尼松逐渐缓慢减量,每周使用环磷酰胺0.4g(累积7.2g);
华法林抗凝3mg及3.75mg交替维持INR 1.4-2.4,余心脏方面用药不变;
活动耐力逐步恢复,目前可上2层楼,未再出现憋喘不能平卧或意识丧失。
【随访情况】
患者一直接受密切随访,血常规、尿常规(-),24hUPro 0.12g,便OB(+)×2;肝肾功:Cr 100μmol/L,余正常范围。
心脏相关检查
BNP 96ng/L,cTnI 0.01μg/L;
6个月后超声心动图:节段性室壁运动异常(左室下后壁运动略减低),左房增大,LVEF(M型)60%;(图4 6个月后心电图)
6个月后心肌双核素显像:与之前相比原左室部分下壁中部血流灌注完全恢复正常,下壁基底心肌血流灌注较前明显改善,新出现后侧壁基底部血流灌注轻度受损;PET显像可见心肌存活;
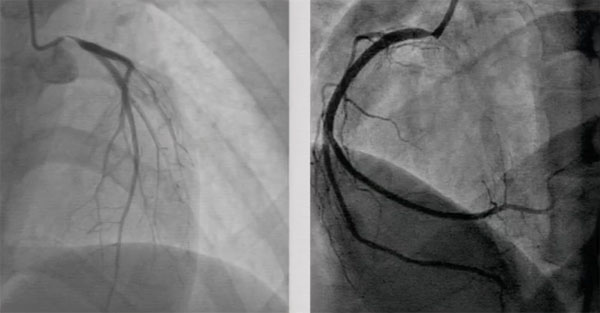
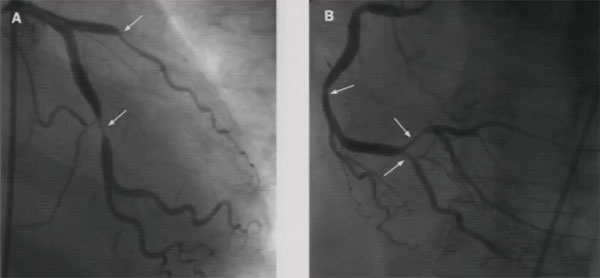
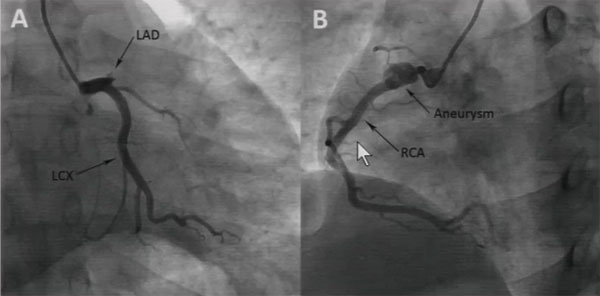
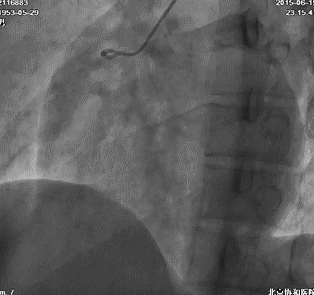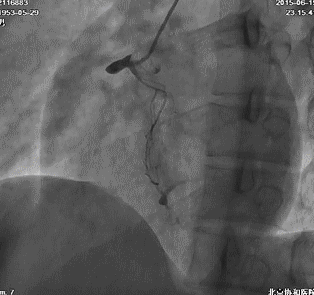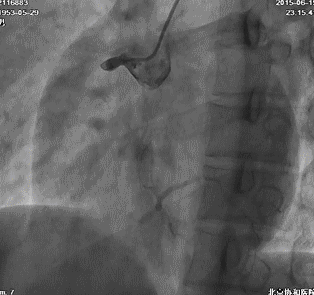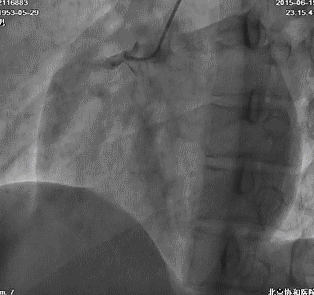
冠脉造影:左主干及LAD、LCX、RCA病变情况与前次类似,侧支循环较前增多。
目前情况
患者可步行200米或上2层楼,但快步行走或扫地等家务活动时仍有胸痛及憋喘,需临时加用硝酸甘油喷雾。
诉左侧大腿内侧感觉异常,尿便正常,无下肢运动障碍。
查体血压116/52mmHg,心率74bpm,SpO2 99% RA,心肺听诊无殊,腹软无压痛未及包块,双下肢不肿,四肢腱反射亢进,右侧为著,右侧Hoffman征及Babinski征(+)。
思考问题
是否再血管化,如果再血管化,CABG还是PCI?
22岁男性,反复意识丧失3年余,活动后胸闷2年余,加重5月。
现病史
2012年4月行走时突发意识丧失,伴双眼凝视、口吐白沫、肢体抽搐,无舌咬伤、尿便失禁,约1小时意识自行恢复。上述症状于2012年底、2013年中再发2次,外院查脑电图、头颅MRI未见异常。
2013年6月起出现上2~3层楼后胸闷,休息数分钟可缓解,活动耐量进行性减低。
2014年10月卧位休息时再发意识丧失,性质同前,意识恢复后出现言语不利,右侧肢体麻木、肌力下降。外院查:
•BP160-170/110mmHg。心电图:窦性心律,HR 102bpm,II、III、aVF可见小Q波、ST段压低0.05mV、T波倒置。
•尿常规:Pro>3g/L,BLD(-),24小时尿蛋白4.9g;肝肾功(-);免疫球蛋白及补体:IgM↓0.293g/L,C4 0.405↑,余正常;自身抗体均(-)。
•头MRI:左侧中脑大脑脚长T1长T2,DWI高信号,考虑为新发梗死,左侧额叶半卵圆中心白质高信号。肌电图大致正常。
外院考虑“慢性肾小球肾炎,高血压,脑血管病”,予硝苯地平控释片、福辛普利钠降压,他克莫司早2mg/晚1mg治疗肾病,血压波动于140/90mmHg,针灸治疗后肢体活动不利及言语不清逐渐恢复。此后患者活动后胸闷、憋气症状仍进行性加重,2015年初出现步行数十米或上1层楼后胸痛,伴向双上肢放射,休息数分钟后可缓解。
2015年6月1日夜间患者突发胸痛,伴胸闷、憋气,不能平卧,双下肢对称可凹性水肿。cTnI 1.31ng/mL(6月3日)→7.7ng/ml(6月5日),NT-proBNP 778pg/ml。肺部CT:双肺少量斑片影。超声心动图:左室轻度增大,收缩功能减低(LVEF 36%)。予利尿治疗后症状略改善。
6月14日患者床旁活动后出现心前区痛、向双上肢放射伴胸闷、憋气,急诊就诊。查心电图示窦性心动过速,aVR ST段抬高0.2mV,I、aVL、II、aVF、V1-V7 ST段压低,I、aVL、V5-V7 T波双向或倒置,cTnI 1.74~4.67ug/L,考虑急性非ST段抬高心肌梗死,予阿司匹林、氯吡格雷、阿托伐他汀、低分子肝素治疗及硝酸甘油静脉泵入,症状持续2-3小时后缓解,收入CCU。(图1 胸痛发作时心电图)(图2 胸痛缓解时心电图)
既往史
儿时体健,无长期发热病史,2012年初出现发热,Tmax 39℃,伴有右侧腮腺区肿大,半月后出现后背部斑丘疹,伴破溃,20天左右好转;同年夏天出现左侧睾丸疼痛,间断发作,口服迈之灵可缓解。
个人史、家族史
无特殊,病前为校篮球队员。
【体格检查】
BP 120/60mmHg,HR 73bpm,BMI 25.9kg/m2,背部皮肤可见陈旧皮疹遗留色素沉着,腹部紫纹。心肺听诊(-),腹部(-),双侧上肢血压对称,足背动脉搏动双侧未及;右侧Hoffman(+),Babinski(+),左侧上下肢病理征未引出。
【实验室检查】
血常规(-)。
尿常规:PRO TRACE,BLD(-);24小时尿蛋白0.61-1.06g,98%肾小球来源。
肾功能:Cr 80-100μmol/L。
血脂:LDL-C 1.11mmol/L,TC 2.49mmol/L,TG 2.14mmol/L,HDL-C 0.70mmol/L。
心肌酶:cTnI最高6.1μg/L后逐渐下降;BNP 240ng/L。
炎症指标:hsCRP 5.92mg/L;ESR 49mm/h。
免疫指标:C3、C4、IgA、IgG、RF(-),IgM↓0.27g/L;ANA3项、抗ENA抗体、ANCA、LA、抗磷脂抗体谱均(-);乙肝5项:HBeAb、HBcAb、HBsAb(+),HBV-DNA(-)。
【辅助检查】
超声心动图:节段性室壁运动异常(左室下后壁内膜回声增强,无运动,室间隔基部运动减低),左室收缩功能减低,双平面法LVEF 42%,轻度二、三尖瓣关闭不全。
下肢动脉超声:右侧胫前动脉弥漫性狭窄,左侧胫前动脉中下段闭塞可能性大;双上肢超声未见明显狭窄。
腹主动脉CTA:脾动脉及双肾动脉远端管腔轻度狭窄,可见小侧支循环开放。肝总动脉及其分支闭塞,周围多发细小侧支循环开放。肠系膜下动脉起始部及双侧髂内动脉多发管腔不同程度狭窄。考虑血管炎性病变可能;脾脏前下部片状低强化区,脾梗死可能;左肾小片状强化减低影,缺血性改变可能。(图3 腹主动脉CTA)
头颈CTA:右侧椎动脉全程闭塞;余头颈部血管未见明显异常。
神经内科会诊:反复意识丧失考虑癫痫发作,左侧中脑梗死可能为小血管闭塞所致,与高血压或全身血管炎相关。
免疫科会诊:考虑系统性血管炎,结节性多动脉炎可能性大。建议予泼尼松1mg/kg,环磷酰胺0.4g/周,并建议积极冠脉重建。
多科会诊(心外、心内、麻醉科):考虑患者冠脉病变有CABG指征,但病因为血管炎且尚未控制,外科手术风险极高,受益有限。介入治疗方面患者冠脉病变极重,仅一根对角支供应全部冠脉血供,一旦处理前降支导致对角支开口闭塞,治疗风险极大。
入院后逐步减停硝酸甘油泵入,给予阿司匹林100mg qd、氯吡格雷75mg Qd(1个月后停用),低分子肝素→华法林抗凝,单硝酸异山梨酯缓释片60mg qd、尼可地尔5mg tid、盐酸曲美他嗪20mg tid扩冠和改善心肌代谢,酒石酸美托洛尔95mg q12h降低心肌耗氧,福辛普利5mg qd、辛伐他汀20mg qn、呋塞米10mg qd、螺内酯20mg qd。
甲强龙60mg iv qd×7d→泼尼松60mg qd;环磷酰胺0.4g qw。
整体评价后未进行再血管化治疗。
患者病情相对平稳后出院,泼尼松逐渐缓慢减量,每周使用环磷酰胺0.4g(累积7.2g);
华法林抗凝3mg及3.75mg交替维持INR 1.4-2.4,余心脏方面用药不变;
活动耐力逐步恢复,目前可上2层楼,未再出现憋喘不能平卧或意识丧失。
【随访情况】
患者一直接受密切随访,血常规、尿常规(-),24hUPro 0.12g,便OB(+)×2;肝肾功:Cr 100μmol/L,余正常范围。
心脏相关检查
BNP 96ng/L,cTnI 0.01μg/L;
6个月后超声心动图:节段性室壁运动异常(左室下后壁运动略减低),左房增大,LVEF(M型)60%;(图4 6个月后心电图)
6个月后心肌双核素显像:与之前相比原左室部分下壁中部血流灌注完全恢复正常,下壁基底心肌血流灌注较前明显改善,新出现后侧壁基底部血流灌注轻度受损;PET显像可见心肌存活;
冠脉造影:左主干及LAD、LCX、RCA病变情况与前次类似,侧支循环较前增多。
目前情况
患者可步行200米或上2层楼,但快步行走或扫地等家务活动时仍有胸痛及憋喘,需临时加用硝酸甘油喷雾。
诉左侧大腿内侧感觉异常,尿便正常,无下肢运动障碍。
查体血压116/52mmHg,心率74bpm,SpO2 99% RA,心肺听诊无殊,腹软无压痛未及包块,双下肢不肿,四肢腱反射亢进,右侧为著,右侧Hoffman征及Babinski征(+)。
思考问题
是否再血管化,如果再血管化,CABG还是PCI?
0 条评论
版权声明
CMIT周刊版权所有,欢迎个人转发分享,其他任何媒体、网站转载须在醒目位置注明“转自CMIT周刊”。
CMIT周刊版权所有,欢迎个人转发分享,其他任何媒体、网站转载须在醒目位置注明“转自CMIT周刊”。
推荐文章
行业新闻
实时热点

反思|一例PCI术后2月消化道出血辗转多科室的曲折经历
PCI术后消化道大出血,如何联合多学科优化诊疗?如何权衡血栓形成及出血风险?相信不少同道都曾面临这样的两难境地,本期《CMIT周刊》以一则PCI术后2月消化道出血的病例报告为线索,联合...
2017-03-18查看详情+